Российские ученые применили CRISPR/Cas9 для борьбы с повышением сахара в крови
Биологи выяснили, что улучшить состояние клеток, страдающих от избытка глюкозы, можно, заблокировав транспортер VDAC1, который обеспечивает обмен веществ между митохондриями и цитоплазмой. при сахарном диабете количество этих белков значительно возрастает. Это приводит к окислительному стрессу и гибели клеток. Авторы предложили уменьшать число и активность транспортеров с помощью технологии CRISPR/Cas9 и молекул–блокаторов. Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале Antioxidants.
Уровень в крови глюкозы – основной молекулы, из которой наш организм извлекает энергию, – обычно возрастает после приема пищи и довольно быстро (в течение 3–4 часов) снижается до исходного. Однако при нарушении обмена веществ, например сахарном диабете, концентрация глюкозы постоянно остается высокой, и это состояние называют гипергликемией. Она негативно сказывается на многих органах, увеличивая риск сердечно–сосудистых заболеваний, поражения нервов, разрушения костей и проблем со зрением. Этот эффект связывают с тем, что избыток глюкозы приводит к нарушению окислительно–восстановительных процессов в клетках из–за повреждения митохондрий – «энергетических станций» клетки.
Между митохондриями и остальной клеткой происходит постоянный обмен питательными веществами и сигнальными молекулами, который обеспечивают «встроенные» в мембрану митохондрий белки–транспортеры семейства VDAC. При сахарном диабете в некоторых органах и тканях их число увеличивается, и это приводит к тому, что в клетку из митохондрии в избыточном количестве начинают поступать активные формы кислорода – молекулы, в высоких концентрациях повреждающие мембраны и ДНК, – а также вещества, стимулирующие программируемую клеточную гибель. Поэтому ученые предполагают, что бороться с негативными последствиями гипергликемии можно, частично заблокировав работу белков VDAC1.
Ученые из Марийского государственного университета с коллегами проверили эту гипотезу. Они использовали в экспериментах культуры эндотелиоцитов мышей – клеток, выстилающих стенки сосудов, – а также фибробластов человека – клеток соединительной ткани. Исследователи протестировали два подхода. В первом случае биологи с помощью технологии геномного редактирования CRISPR/Cas9 «выключили» ген, кодирующий белок VDAC1. В результате в полученных клетках осталось только 10% белка от нормы. Во втором случае клеточные культуры просто обработали молекулой–ингибитором, связывающейся с белковыми каналами VDAC1 и блокирующей их. Затем все клетки помещали на 36 часов в раствор глюкозы для создания условий гипергликемии. В качестве контроля использовались культуры, в которых уровень VDAC1 не изменяли.
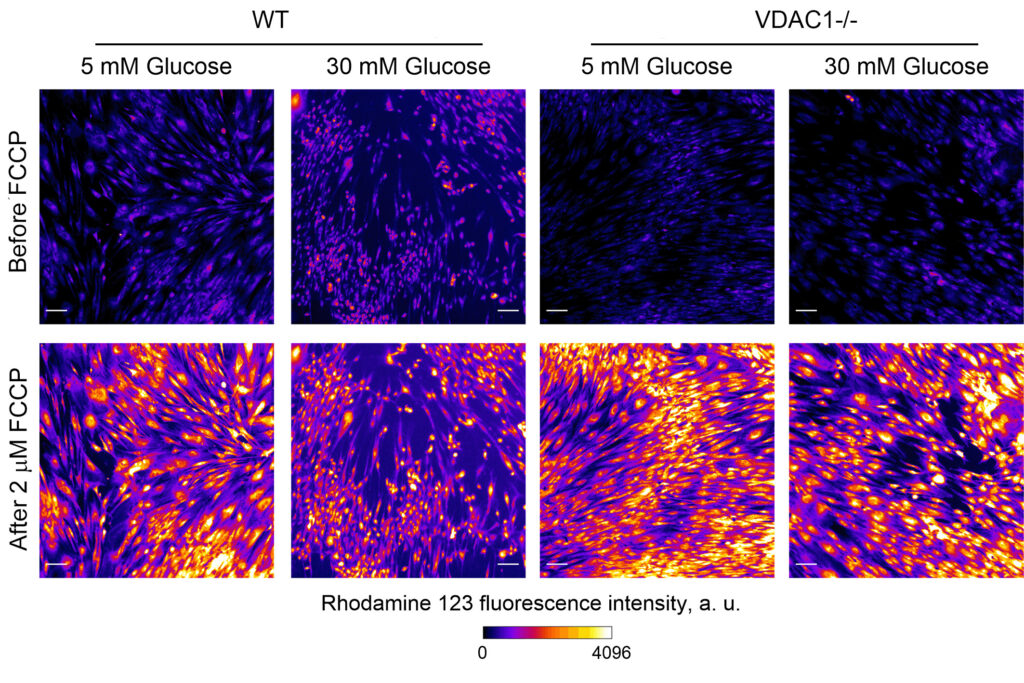
Биологи сравнили состояние клеток и работу митохондрий в каждом случае, подкрашивая интересующие структуры и молекулы флуоресцентными («светящимися») красителями. Оказалось, что митохондрии со сниженным количеством каналов VDAC1 производили почти в полтора раза меньше активных форм кислорода по сравнению с контрольной группой, что пропорционально уменьшало негативное влияние на клетки и риск их гибели от окислительного стресса.
Кроме того, исследование показало, что при гипергликемии в клетках снижается активность генов, участвующих в увеличении количества митохондрий. Это может привести к нехватке энергии, необходимой для нормальной работы клеток. В случаях, когда ген VDAC1 был заблокирован с помощью технологии CRISPR/Cas9, этот негативный эффект пропадал.
«Снизив количество или активность транспортеров VDAC1 в мембране митохондрий, действительно можно добиться улучшения состояния клеток при гипергликемии. Потенциально наши результаты могут лечь в основу создания новых лекарственных препаратов для терапии диабета», – рассказывает руководитель проекта, проректор по инновационной деятельности Марийского государственного университета Константин Белослудцев.
В дальнейшем авторы планируют протестировать другие способы блокировки белков VDAC1, чтобы понять, какой подход позволит наиболее эффективно бороться с последствиями гипергликемии.
Фото: Изменение мембранного потенциала митохондрий в фибробластах кожи человека с нормальной (WT) и пониженной (VDAC1–/–) экспрессией VDAC1 в условиях нормо– и гипергликемии до и после добавки молекулы–разобщителя. Источник: Константин Белослудцев